variabilidade e indeterminaldade de espectros conforme o sistema decadimensional e categorial Graceli.
+
x
decadimensional
x
T l T l E l Fl dfG l
N l El tf l
P l Ml tfefel
Ta l Rl
Ll
D
É interessante notar que, ainda no primeiro artigo de sua trilogia, além das demonstrações indicadas acima, Bohr também demonstrou que, se o momento angular (M) de um elétron em movimento circular (de raio a) em torno do núcleo de um átomo, tivesse o valor dado por  , com
, com  , a energia desse elétron seria estacionária, isto é, o elétron estaria em um estado quântico de energia bem definido. Aliás, registre-se que a “quantização do momento angular” já havia sido sugerida pelo físico inglês John William Nicholson (1881-1955), em 1912 (Monthly Notices of the Royal Astronomical Society 72, pgs. 49; 139; 677; 693; 729), em seus trabalhos nos quais desenvolveu seu modelo atômico “tipo saturniano”, isto é: um caroço central carregado positivamente rodeado de anéis eletrônicos.
, a energia desse elétron seria estacionária, isto é, o elétron estaria em um estado quântico de energia bem definido. Aliás, registre-se que a “quantização do momento angular” já havia sido sugerida pelo físico inglês John William Nicholson (1881-1955), em 1912 (Monthly Notices of the Royal Astronomical Society 72, pgs. 49; 139; 677; 693; 729), em seus trabalhos nos quais desenvolveu seu modelo atômico “tipo saturniano”, isto é: um caroço central carregado positivamente rodeado de anéis eletrônicos.
Uma das primeiras confirmações experimentais do modelo atômico de Bohr foi conseguida por intermédio da experiência realizada pelos físicos alemães James Franck (1882-1964; PNF, 1925) e Gustav Ludwig Hertz (1887-1975; PNF, 1925) [sobrinho do famoso físico alemão Heinrich Rudolf Hertz (1857-1894), que havia obtido, em 1887, as hoje famosas “ondas Hertzianas” – microondas]. Vejamos como isso aconteceu. Desde 1911, esses físicos realizavam experiências sobre descargas elétricas nos gases, procurando uma relação entre a Teoria Quântica de Planck e o potencial de ionização dos gases utilizados. Esse potencial representava a diferença de potencial (V) que devia ser aplicada aos raios catódicos (elétrons) com o objetivo de ionizar, por colisão, os átomos dos gases considerados. Até 1913, eles haviam conseguido medir os potenciais de ionização de diversos gases [hidrogênio (H), hélio (He), neon (Ne), oxigênio (O) etc.], usando aquela técnica. No entanto, em 1914 (Verhandlungen der Deustschen Physikalische Gesellschaft 16, pgs. 457; 512), eles encontraram um resultado surpreendente, comunicado por Hertz na reunião daSociedade Alemã de Física realizada no dia 24 de abril de 1914. Tal resultado deveu-se ao seguinte.
A experiência que Franck e Hertz realizaram relacionava-se com o estudo da colisão de elétrons com vapor de mercúrio (Hg) à pressão de cerca de 1 mm de Hg. Por intermédio de um amperímetro, eles mediram a corrente elétrica do anodo [folha cilíndrica de platina (Pt)] em função do potencial acelerador aplicado ao catodo (fio de platina incandescente). Com isso, eles estudaram a velocidade (v) dos elétrons (de massa m e carga e) antes e depois da colisão com os átomos de Hg, por intermédio da expressão:  . Observaram, então, que a corrente elétrica aumentava com o potencial (V) até quando este atingia o valor aproximado de 4,9 V (Volts), caindo a corrente rapidamente após aquele valor do potencial. No entanto, à medida que o potencial crescia novamente, a corrente voltava também a crescer até quando o potencial atingisse o valor aproximado do dobro do valor anterior (9,8 V), quando de novo a corrente caía de maneira brusca. Esse comportamento corrente versus potencial repetia-se sempre que o potencial fosse um múltiplo em torno de 4,9 V, indicando que o elétron poderia sofrer mais de uma colisão inelástica com o vapor de Hg. Esses valores críticos do potencial eram acompanhados pela emissão de luz de comprimento de onda de 2.536 Ǻ. Franck e Hertz encontraram um comportamento similar, embora menos pronunciado, quando substituíram o vapor de Hg por He, sendo o potencial crítico deste em torno de 21 V.
. Observaram, então, que a corrente elétrica aumentava com o potencial (V) até quando este atingia o valor aproximado de 4,9 V (Volts), caindo a corrente rapidamente após aquele valor do potencial. No entanto, à medida que o potencial crescia novamente, a corrente voltava também a crescer até quando o potencial atingisse o valor aproximado do dobro do valor anterior (9,8 V), quando de novo a corrente caía de maneira brusca. Esse comportamento corrente versus potencial repetia-se sempre que o potencial fosse um múltiplo em torno de 4,9 V, indicando que o elétron poderia sofrer mais de uma colisão inelástica com o vapor de Hg. Esses valores críticos do potencial eram acompanhados pela emissão de luz de comprimento de onda de 2.536 Ǻ. Franck e Hertz encontraram um comportamento similar, embora menos pronunciado, quando substituíram o vapor de Hg por He, sendo o potencial crítico deste em torno de 21 V.
Para interpretar tais resultados, Franck e Hertz utilizaram as idéias apresentadas pelo físico alemão Johannes Stark (1874-1957; PNF, 1919) sobre a origem das séries espectrais. Em 1908 (Physikalische Zeitschrift 9, p. 85), Stark propôs um modelo segundo o qual as séries espectrais se relacionavam com o processo de ionização de átomos e moléculas, e que sua freqüência ( ) era ligada ao potencial de ionização (V) através da expressão:
) era ligada ao potencial de ionização (V) através da expressão:  . Portanto, para Franck e Hertz, logo que a energia cinética do elétron (
. Portanto, para Franck e Hertz, logo que a energia cinética do elétron (
 ) atingia a energia potencial crítica (eV), uma parte dela era usada na ionização e a outra era emitida como luz de freqüência
) atingia a energia potencial crítica (eV), uma parte dela era usada na ionização e a outra era emitida como luz de freqüência  . Com esse procedimento, eles chegaram a obter o valor de
. Com esse procedimento, eles chegaram a obter o valor de  , em bom acordo com os valores experimentais até então conhecidos.
, em bom acordo com os valores experimentais até então conhecidos.
+
x
decadimensional
x
T l T l E l Fl dfG l
N l El tf l
P l Ml tfefel
Ta l Rl
Ll
D
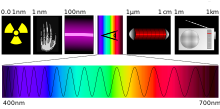
No âmbito científico um espectro é uma representação das amplitudes ou intensidades - o que geralmente traduz-se por energia - dos componentes ondulatórios de um sistema quando discriminadas uma das outras em função de suas respectivas frequências (ou comprimentos de onda). Em um espectro as componentes ondulatórias (fases) distinguem-se fisicamente umas das outras não por suas naturezas mas sim pelas suas frequências, portanto. O exemplo típico é o espectro visível.
Caso o diagrama expresse a frequência associada a cada componente ondulatória do sistema como função do respectivo comprimento de onda e não a intensidade como função da frequência tem-se o que se denomina em física por relação de dispersão. Relações de dispersão e espectros, apesar de distintos, encontram-se relacionados, visto que, entre outras observações, as intensidades em um espectro podem ser descritas, via relação de dispersão, tanto em função das frequências como em função dos respectivos comprimentos de onda a elas associados.
O conceito de espectro também aplica-se à dinâmica de um feixe material em virtude da dualidade partícula-onda. Associado à partícula material em movimento há uma onda de matéria cuja frequência mostra-se diretamente proporcional à sua energia cinética. Relações estabelecidas em função das energias cinéticas são em essência relações estabelecidas em função das frequências das ondas de matéria associadas; e assim também constituem exemplos de espectros. Como exemplo têm-se os espectros "XPS", obtidos via processo de espectroscopia de fotoelétrons excitados por raios X.
Um equipamento capaz de analisar e gerar o espectro de um sinal temporalmente complexo contudo "bem comportado" [1] é denominado espectrômetro. Se acrescido de funcionalidade que lhe permita gerar um registro fotográfico do espectro exibido, o equipamento denomina-se espectrógrafo [2]. Em termos teóricos, a ferramenta matemática que extrai de um sinal no domínio do tempo cada uma das componentes espectrais que, juntas, o caracterizam no domínio da frequência, é a transformada de Fourier. O sinal também pode ser integralmente reescrito no domínio tempo via suas componentes no domínio da frequência através da série de Fourier.
Espectro de massa[editar | editar código-fonte]
Um exemplo típico de um espectrômetro é um espectrômetro de massa. Valendo-se entre outros da propriedade elétricasassociadas às partículas e aos núcleos atômicos, uma dada mistura de isótopos de um elemento químico ou mesmo elementos químicos distintos é inicialmente vaporizada, ionizada, colimada em um feixe de partículas feito mover-se à uma velocidade pré-estabelecida, e então dirigida para uma região onde campos magnéticos fazem-nas descrever trajetórias semicirculares com raios que dependem explicitamente de seus momentos e, por conseguinte, explicitamente de suas massas ou energias cinéticas. Sensores ao final possibilitam a construção de um gráfico discriminando a percentagem estequiométrica em massa de cada componente na mistura inicial em função da massa - ou por vezes, devido a detalhes técnicos, em função da razão carga / massa - do respectivo componente.
A denominação "espectro" se justifica aqui em função da dualidade partícula-onda. De Broglie trouxe à luz o fato de que partículas massivas têm comportamento ondulatório, onde seus comprimento de onda encontram-se relacionados aos seus momentos, ao passo que, sob a mesma ótica, Max Planck mostrou que as energias das partículas quânticas em movimento encontram-se relacionadas às frequências das ondas de matéria à estas associadas. Separar as partículas por massa traduz-se de forma prática em tal sistema em discriminá-las através de suas energias cinéticas, ou, via dualidade partícula-onda, decompor a massa total da amostra em função das frequências associadas a seus respectivos elementos constituintes quando em movimento. Via relação de dispersão, o mesmo raciocínio pode ser feito com base nos momentos, ou seja, com base nos associados comprimentos de onda.
Espectro eletromagnético e óptico[editar | editar código-fonte]
O exemplo mais expressivo de um espectro é o padrão obtido quando as radiações electromagnéticas são primeiro espacialmente discriminadas em função de suas frequências - mediante algum fenômeno físico explicitamente dependente da última grandeza, a exemplo o que ocorre quando as ondas transitam de um meio de propagação para outro onde a relação de dispersão mostre-se distinta da primeira (refração) - e são então devidamente projetadas sobre filme adequadamente sensível às intensidades destas. Se a radiação eletromagnética encontra-se na faixa do visível, as diversas frequências eletromagnéticas traduzem-se em "cores" visualmente observáveis, e para o caso onde todas as componentes na faixa de frequências em questão estejam significativamente presentes, tem-se a impressão de um arco-iris.
A exemplo, as radiações solares resultam em um espectro de bandas coloridas quando a luz branca passa através de um prisma ou rede de difração. As cores deste espectro, ordenadas por comprimentos de onda decrescentes (ou frequências crescentes), são: vermelho, laranja, amarelo, verde, azul, anil e violeta. A busca por maiores detalhes quanto à radiação solar leva ao Espectro de Fraunhofer.
Os espectros formados a partir de radiações emitidas por corpos incandescentes ou convenientemente excitados são designados por espectros de emissão.
Quando a luz branca passa através de um meio semitransparente, dá-se uma absorção selectiva de radiações de certos comprimentos de onda; o espectro da radiação transmitida designa-se então por espectro de absorção.
Os espectros de emissão e de absorção de uma substância são característicos dessa substância, sendo muitas vezes usados para a sua identificação. Tais espectros são o resultado de transições entre diferentes autoestados dos átomos ou moléculas da substância, sendo emitidas ou absorvidas, dinamicamente, ondas electromagnéticas.
A frequência f das radiações emitidas ou absorvidas é dada por , onde E1 e E2 são as energias, respectivamente, dos estados inicial e final entre os quais deu-se a transição, usualmente eletrônica, e h é a constante de Planck. Quando E1 é maior que E2, ondas electromagnéticas (fótons) são emitidas; no caso contrário, fótons são absorvidos.
Espectro contínuo é aquele em que figuram com intensidades não nulas todos os comprimentos de onda presentes na faixa em estudo. As radiações emitida por um corpo negro, a exemplo as emitidas por lâmpadas incandescentes, se decompõem em espectros desta natureza.
Espectro de riscas, também chamados espectros de raias, são, ao contrário, aqueles em que aparecem apenas certos comprimentos de ondas específicos, não havendo energia associada aos demais comprimentos de onda. Espectros oriundos de lâmpadas fluorescentes são desta natureza.
Espectros Atômicos[editar | editar código-fonte]
Espectros atômicos são espectros de raias. Um dos espectros atômicos mais estudados, entre outros dada a sua importância em áreas como mecânica quântica, física de plasmas, astrofísica, astronomia e cosmologia, é o espectro do hidrogênio, tanto atômico quanto molecular. Quando a estrutura fina é ignorada, os comprimentos de onda para os quais verificam-se amplitudes não nulas ou negligenciáveis (radiação espúria) no espectro do hidrogênio atômico são determináveis por uma relação matemática empírica conhecida como fórmula de Rydberg:
Onde
A análise do átomo de hidrogênio é de suma importância para a compreensão da estrutura da matéria por ser esse o único átomo para o qual se estabelece uma descrição matemática analítica precisa; sendo por esse motivo o modelo escolhido para se introduzir o tratamento quântico da matéria na maioria dos (para não dizer em todos os) livros didáticos acerca do assunto. A solução da Equação de Schrödinger sujeita ao potencial de interação couloumbiano adequado ao átomo fornece por solução autoestados de energia descritos por autofunções e autovalores dos quais se derivam conclusões lógicas em plenitude condizentes com a estrutura espectral e demais dados empiricamente obtidos para o elemento (os autovalores de energia mais importantes, e transições esperadas, são mostrados na figura ao lado).
As autofunções do átomo de hidrogênio estabelecem uma base mediante a qual todos os demais átomos da tabela são, por aproximação, matematicamente descritos; sendo as correspondentes soluções para cada átomo obtidas por ténicas de solução numéricas e não por soluções analíticas, a exemplo via método desenvolvidos por Douglas Hartree(Teoria de Hartree). A partir dos resultados de tal teoria consegue-se então determinar matematicamente as características dos espectros esperados para os demais átomos da tabela periódica.
as dimensões categorias podem ser divididas em cinco formas diversificadas.
tipos, níveis, potenciais, tempo de ação, especificidades de transições de energias, de fenômenos, de estados de energias, físicos [estruturais], de fenômenos, estados quântico, e outros.
paradox of the system of ten dimensions and categories of Graceli.
a four-dimensional system can not define all the energies, changes of structures, states and phenomena within a structure, that is why there are ten or more dimensions, I have developed and I work with ten, but nature certainly goes beyond ten, with this we move to a decadimensional and categorial universe.
that is, categories ground the variables of phenomena and their interactions and transformations.
and with this we do not have a relationship with mass, but with structure, therefore, a structure carries with it much more than mass, since also mass is related to forces, inertia, resistances and energies.
but structures are related to transitions of physical states, quantum, energies, phenomena, and others.
as well as transitions of energies, phenomena, categories and dimensions.
paradoxo do sistema de dez dimensões e categorias de Graceli.
um sistema de quatro dimensões não tem como definir todas as energias, mudanças de estruturas, estados e fenômenos dentro de uma estrutura, por isto se tem dez ou mais dimensões, desenvolvi e trabalho com dez, mas a natureza com certeza vai alem das dez, com isto caminhamos para um universo decadimensional e categorial.
ou seja, as categorias fundamentam as variáveis dos fenõmenos e suas interações e transformações.
e com isto não se tem uma relação com massa, mas com estrutura, pois, uma estrutura carrega consigo muito mais do que massa, uma vez também que massa está relacionado com forças, inércia, resistências e energias.
mas estruturas está relacionado com transições de estados físicos, quântico, de energias, de fenômenos, e outros.
como também transições de energias, fenômenos, categorias e dimensões.
a four-dimensional system can not define all the energies, changes of structures, states and phenomena within a structure, that is why there are ten or more dimensions, I have developed and I work with ten, but nature certainly goes beyond ten, with this we move to a decadimensional and categorial universe.
that is, categories ground the variables of phenomena and their interactions and transformations.
and with this we do not have a relationship with mass, but with structure, therefore, a structure carries with it much more than mass, since also mass is related to forces, inertia, resistances and energies.
but structures are related to transitions of physical states, quantum, energies, phenomena, and others.
as well as transitions of energies, phenomena, categories and dimensions.
paradoxo do sistema de dez dimensões e categorias de Graceli.
um sistema de quatro dimensões não tem como definir todas as energias, mudanças de estruturas, estados e fenômenos dentro de uma estrutura, por isto se tem dez ou mais dimensões, desenvolvi e trabalho com dez, mas a natureza com certeza vai alem das dez, com isto caminhamos para um universo decadimensional e categorial.
ou seja, as categorias fundamentam as variáveis dos fenõmenos e suas interações e transformações.
e com isto não se tem uma relação com massa, mas com estrutura, pois, uma estrutura carrega consigo muito mais do que massa, uma vez também que massa está relacionado com forças, inércia, resistências e energias.
mas estruturas está relacionado com transições de estados físicos, quântico, de energias, de fenômenos, e outros.
como também transições de energias, fenômenos, categorias e dimensões.
= entropia reversível
postulado categorial e decadimensional Graceli.
TUDO QUE ESTÁ RELACIONADO COM ENERGIA, ESTRUTURAS, FENÔMENOS E DIMENSÕES ESTÁ INSERIDO NO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.
todo sistema decadimensional e categorial é um sistema transcendente e indeterminado.
TUDO QUE ESTÁ RELACIONADO COM ENERGIA, ESTRUTURAS, FENÔMENOS E DIMENSÕES ESTÁ INSERIDO NO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.
todo sistema decadimensional e categorial é um sistema transcendente e indeterminado.
T l T l E l Fl dfG l
N l El tf l
P l Ml tfefel
Ta l Rl
Ll
D
1] Cosmic space.
2] Cosmic and quantum time.
3] Structures.
4] Energy.
5] Phenomena.
6] Potential.
7] Phase transitions of physical [amorphous and crystalline] states and states of energies and phenomena of Graceli.
8] Types and levels of magnetism [in paramagnetic, diamagnetic, ferromagnetic] and electricity, radioactivity [fissions and fusions], and light [laser, maser, incandescence, fluorescence, phosphorescence, and others.
9] thermal specificity, other energies, and structure phenomena, and phase transitions.
10] action time specificity in physical and quantum processes.
2] Cosmic and quantum time.
3] Structures.
4] Energy.
5] Phenomena.
6] Potential.
7] Phase transitions of physical [amorphous and crystalline] states and states of energies and phenomena of Graceli.
8] Types and levels of magnetism [in paramagnetic, diamagnetic, ferromagnetic] and electricity, radioactivity [fissions and fusions], and light [laser, maser, incandescence, fluorescence, phosphorescence, and others.
9] thermal specificity, other energies, and structure phenomena, and phase transitions.
10] action time specificity in physical and quantum processes.
Sistema decadimensional Graceli.
1]Espaço cósmico.
2]Tempo cósmico e quântico.
3]Estruturas.
4]Energias.
5]Fenômenos.
6]Potenciais., e potenciais de campos, de energias, de transições de estruturas e estados físicos, quãntico, e estados de fenômenos e estados de transições, transformações e decaimentos.
7]Transições de fases de estados físicos [amorfos e cristalinos] e estados de energias e fenômenos de Graceli.
8]Tipos e níveis de magnetismo [em paramagnéticos, diamagnético, ferromagnéticos] e eletricidade, radioatividade [fissões e fusões], e luz [laser, maser, incandescências, fluorescências, fosforescências, e outros.
9] especificidade térmica, de outras energias, e fenômenos das estruturas, e transições de fases.
10] especificidade de tempo de ações em processos físicos e quântico.
T l T l E l Fl dfG l
N l El tf l
P l Ml tfefel
Ta l Rl
Ll
D
Matriz categorial de Graceli.
T l T l E l Fl dfG l
N l El tf l
P l Ml tfefel
Ta l Rl
Ll
Dl
Tipos, níveis, potenciais, tempo de ação, temperatura, eletricidade, magnetismo, radioatividade, luminescências, dinâmicas, estruturas, fenômenos, transições de fenômenos e estados físicos, e estados de energias, dimensões fenomênicas de Graceli.
[estruturas: isótopos, partículas, amorfos e cristalinos, paramagnéticos, dia, ferromagnéticos, e estados [físicos, quântico, de energias, de fenômenos, de transições, de interações, transformações e decaimentos, emissões e absorções, eletrostático, condutividade e fluidez]].
trans-intermecânica de supercondutividade no sistema categorial de Graceli.
EPG = d [hc] [T / IEEpei [pit] = [pTEMRLD] and [fao] [itd] [iicee] tetdvd [pe] cee [caG].]
p it = potentials of interactions and transformations.
Temperature divided by isotopes and physical states and potential states of energies and isotopes = emissions, random wave fluxes, ion interactions, charges and energies structures, tunnels and entanglements, transformations and decays, vibrations and dilations, electrostatic potential, conductivities, entropies and enthalpies. categories and agents of Graceli.
h e = quantum index and speed of light.
[pTEMRlD] = THERMAL, ELECTRICAL, MAGNETIC, RADIOACTIVE, Luminescence, DYNAMIC POTENTIAL] ..
EPG = GRACELI POTENTIAL STATUS.
[pTFE] = POTENCIAL DE TRANSIÇÕES DE FASES DE ESTADOS FÍSICOS E DE ENERGIAS E FANÔMENOS [TRANSIÇÕES DE GRACELI]
, [pTEMRLD] [hc] [pI] [PF] [pIT][pTFE] [CG].
EPG = d [hc] [T / IEEpei [pit] = [pTEMRLD] and [fao] [itd] [iicee] tetdvd [pe] cee [caG].]
p it = potentials of interactions and transformations.
Temperature divided by isotopes and physical states and potential states of energies and isotopes = emissions, random wave fluxes, ion interactions, charges and energies structures, tunnels and entanglements, transformations and decays, vibrations and dilations, electrostatic potential, conductivities, entropies and enthalpies. categories and agents of Graceli.
h e = quantum index and speed of light.
[pTEMRlD] = THERMAL, ELECTRICAL, MAGNETIC, RADIOACTIVE, Luminescence, DYNAMIC POTENTIAL] ..
EPG = GRACELI POTENTIAL STATUS.
[pTFE] = POTENCIAL DE TRANSIÇÕES DE FASES DE ESTADOS FÍSICOS E DE ENERGIAS E FANÔMENOS [TRANSIÇÕES DE GRACELI]
, [pTEMRLD] [hc] [pI] [PF] [pIT][pTFE] [CG].